CAR-T细胞治疗(Chimeric Antigen Receptor T-Cell Therapy)作为一种“活细胞药物”,近年来不仅在血液肿瘤治疗中实现了治愈奇迹,更在系统性红斑狼疮(SLE)、系统性硬化症等自身免疫性疾病重症治疗中展现出颠覆性的疗效。然而,传统CAR-T疗法依赖体外制备,流程繁琐且昂贵。因此像接种疫苗一样,打一针就能在病患体内自动生成CAR-T细胞,从而实现对疾病的长期控制甚至治愈成为了领域内追逐的目标。
2026年2月3日,西湖实验室、昌平实验室马丽佳团队联合南京大学模式动物研究所李颜团队在VITA发表了题为 "An AAV variant enables human T cell engineering in vivo" 的研究论文。该研究首次报道了一种能够高度特异性靶向人T细胞的腺相关病毒(AAV)变体—AAV6-M2。研究团队利用该载体在红斑狼疮(SLE)人源化小鼠模型中,实现了“单针给药”体内生成CAR-T细胞,成功清除致病B细胞并逆转了狼疮肾炎等器官损伤。这一突破性成果不仅解决了AAV载体肝脏毒性的瓶颈,更将CAR-T疗法从复杂的“个性化定制”转化为通用的“货架型基因药物”,为自身免疫疾病的治疗开辟了全新路径。

从“体外制造”到“体内生成”,CAR-T治疗惠及大众的希望
传统的CAR-T细胞治疗(ex vivo CAR-T)需要从患者体内采集T细胞,在体外进行基因改造和扩增后再回输。尽管该疗法在治疗血癌,以及复发/难治性红斑狼疮(SLE)等自身免疫疾病中展现出巨大潜力—即通过彻底清除致病B细胞,能够实现长期的无药缓解,但其推广面临重重困难:
1、高昂的成本与复杂的工艺:个性化制备周期长,且对GMP生产环境要求高导致成本居高不下,难以标准化和规模化以降低治疗成本。
2、患者负担:回输前通常需要进行淋巴细胞清除化疗(Lymphodepletion),给患者带来额外的身体痛苦和感染风险。
与之相比,体内(in vivo)CAR-T技术被视为下一代细胞治疗的“圣杯”。它利用病毒或非病毒载体将CAR基因直接递送至患者体内的T细胞,省去了体外制备环节,使CAR-T疗法变为一种立等可取的“注射药物”,将极大降低治疗门槛和成本。
基于AI进化出的人T细胞靶向变体—AAV6-M2
为了寻找能精准“送货”到人T细胞的载体,马丽佳团队通过AI辅助设计构建了庞大的AAV衣壳蛋白VP3突变文库,通过高通量筛选,成功进化出AAV6-M2这一超级变体。
为了揭示AAV6-M2为何能如此高效地识别T细胞,研究团队综合运用全基因组CRISPR筛选、冷冻电镜(cryo-EM)结构解析及分子对接技术,发现AAV6-M2能够特异性结合T细胞表面的CD62L(L-selectin)分子。因为CD62L主要表达在初始T细胞(Naïve T)和中央记忆T细胞(TCM)表面,这意味着AAV6-M2介导生成的CAR-T细胞具备更强的扩增潜力和更持久的体内续航能力。另外,与传统方法不同,AAV6-M2无需预先激活T细胞即可完成转导,这一特性对于保持体内T细胞的天然功能至关重要。
单针AAV体内生成CAR-T,逆转红斑狼疮(SLE)病程
为了验证AAV体内生成CAR-T的能力,李颜团队通过免疫系统人源化小鼠模型(Human Immune System Mice,HIS mice),验证仅需单次静脉注射AAV6-M2-CD19CAR,在体内多器官中(尤其在骨髓和脾中)高效生成了CAR-T细胞,在AAV注射后第6周后仍维持最高77.5%的CAR-T水平。无论是血液循环中的B细胞,还是躲藏在骨髓、脾脏等组织中的深层B细胞,均被高效清除。
随后,在还原典型狼疮症状的人源化小鼠模型中,验证了单针AAV6-M2的in vivo CAR-T治疗效果。治疗组小鼠的抗双链DNA(anti-dsDNA)和抗Sm抗体等自身抗体水平显著下降;狼疮肾炎症状得到明显改善,肾小球IgG沉积减少,尿素氮(BUN)和肌酐(CREA)水平恢复正常;肺部和肝脏的炎症浸润也完全消失。
这一结果有力证明,AAV6-M2介导的体内CAR-T疗法具备“单次给药、全身起效、深度缓解”的临床转化潜力。
显著的“脱肝”效应,降低传统AAV基因治疗安全性顾虑
安全性是AAV基因治疗面临的最大挑战之一,尤其是野生型AAV容易在肝脏大量富集,引发肝毒性。 本研究发现,得益于衣壳表面的电荷改变,AAV6-M2展现出卓越的肝脏脱靶(Liver De-targeting)特性:在小鼠和非人灵长类(食蟹猴)模型中,AAV6-M2在肝脏中的病毒基因组残留较野生型AAV降低了两个数量级(>100倍)以上。这不仅大幅降低了潜在的肝脏毒性风险,也意味着更多的病毒载体能被有效利用于靶向T细胞,提高了治疗的效费比。
总结与展望
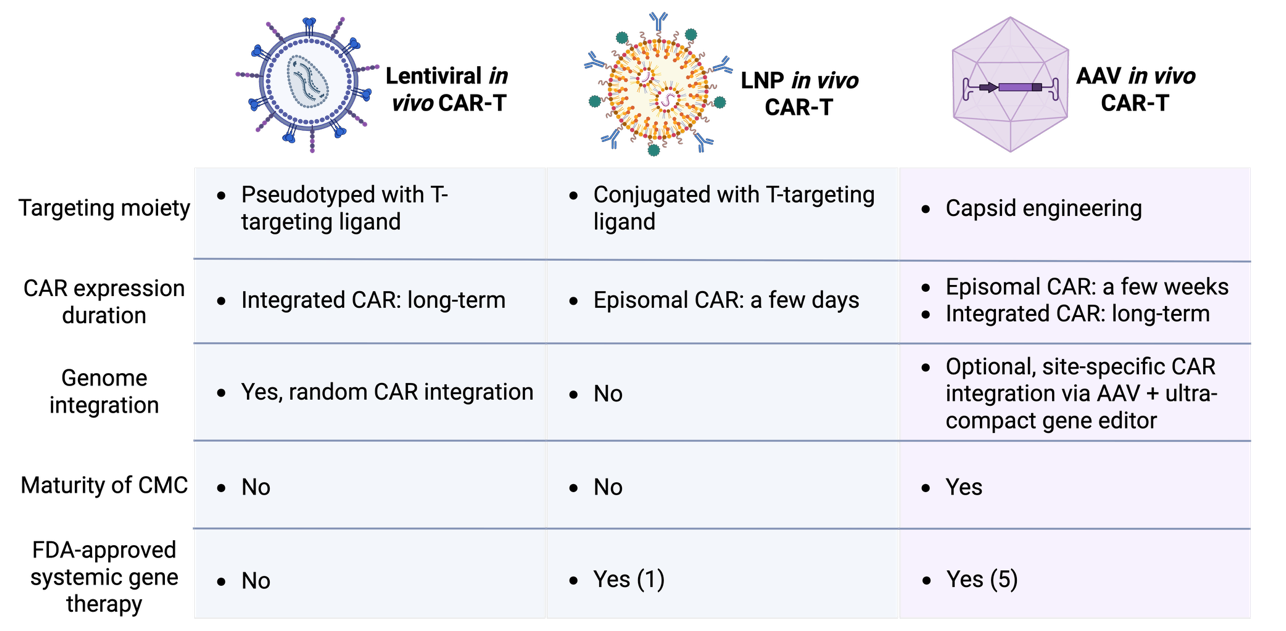
本研究开发了一种高度靶向人T细胞且具备优异肝脏安全性的AAV载体—AAV6-M2,并在人源化小鼠模型中验证了其高效生成in vivo CAR-T实现疾病治疗的可行性。这项工作提供了一种除慢病毒(LV)和脂质纳米颗粒(LNP)之外,更为安全、持久的体内CAR-T递送新方案,并展示了AAV载体不仅适用于治疗罕见遗传病,更可作为通用平台,通过体内细胞工程化技术,进军自身免疫疾病与肿瘤等疾病的广阔市场。
相关论文链接:https://www.vita-journal.com/vita/EN/10.15302/vita.2026.01.0008
图文来源:李颜实验室
责任编辑:张谨



