病毒感染往往起始于一次暴露事件,例如登革热的蚊虫叮咬、狂犬病的动物咬伤、不安全的性行为和共用注射器传播的HIV或HCV,以及呼吸道病毒引发的社区暴发等。在这些情况下,若能在早期主动使用抗病毒药物,通常可以有效阻止感染。然而,现有的预防药物存在一些问题:以HIV为例,常用的抗逆转录病毒药物作用时间短,需要连续服用28天。由于依从性差,预防效果往往不理想。因此,开发一次给药即可快速起效、并能长期发挥作用的抗病毒药物,对保护高危人群具有重要意义。
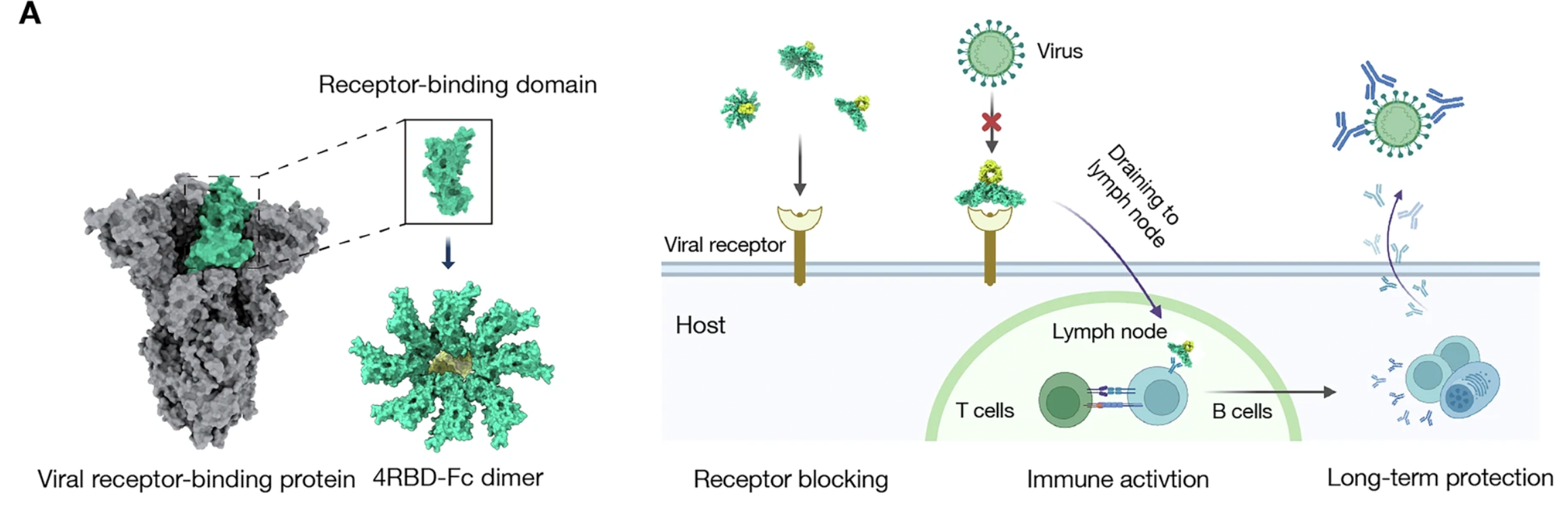
近日,南京大学模式动物研究所李颜教授团队、南京大学生命科学学院董咸池教授团队和中山大学中山医学院邓凯教授团队合作,在 Communications Biology 发表研究论文 “Single-dose infusion of engineered viral receptor binding domain confers rapid and durable protection against viral infection”。研究首次提出并验证了一种新型策略:利用病毒的“受体结合域(RBD)”本身作为药物。通过工程化改造,这种RBD在体内既能迅速占据宿主受体,阻断病毒入侵,又能同时诱导机体产生针对病毒RBD的免疫反应,从而实现“即时+长效”的双重保护。

研究团队的核心思路是:相比传统小分子或抗体药物,完整的RBD更容易精准“抢占”病毒受体,同时还能刺激强有力的抗体反应。这样一来,药物效果不再依赖单次作用,而是通过激活适应性免疫系统而得到延续。
作为概念验证,研究人员选择了SARS-CoV-2。该病毒的RBD结构清晰,与ACE2受体结合的亲和力达到纳摩尔水平,同时包含多个免疫优势表位,可引发强烈的中和抗体反应。为了实现快速阻断与有效免疫激活,研究团队基于结构设计对RBD进行工程化改造,通过多聚化和Fc修饰,增强了其受体结合能力和免疫原性。
最终,他们构建了名为 4RBD-Fc 的RBD多聚体。该分子不仅对ACE2的亲和力更高、稳定性更好,还在体外实验中显示出阻断多种SARS-CoV-2变异株感染的能力。在K18-hACE2小鼠中,鼻内给药的4RBD-Fc能够在肺组织中稳定存在至少7天。更令人关注的是,仅需一次给药,4RBD-Fc就能保护小鼠抵御多次致死剂量的Delta变异株攻击。
机制研究发现,鼻内给药的4RBD-Fc会选择性分布到呼吸道相关淋巴组织,诱导强效的黏膜和全身免疫反应,其保护效果甚至超过了多次常规疫苗接种。多组学分析还揭示,4RBD-Fc通过与FcRn受体结合,促进跨上皮转运,从而增强了在黏膜组织的分布和免疫激活。换句话说,4RBD-Fc兼具“立即封锁病毒通道”和“长期建立免疫记忆”的双重功能,为暴露前和暴露后的抗病毒预防提供了全新解决方案。
综上,本研究首次证明了工程化RBD作为单次给药抗病毒药物的可行性和有效性,为新一代抗病毒药物的开发提供了重要基础和思路。
该论文由南京大学模式动物研究所李颜教授、南京大学生命科学学院董咸池教授、中山大学中山医学院邓凯教授共同通讯。南京大学模式动物研究所李颜课题组的博士生孙海峤、副研究员任德善、中国科学院植物所童贝、中山大学胡奥等为共同第一作者。
原文链接:https://www.nature.com/articles/s42003-025-08704-6
图文来源:李颜课题组
责任编辑:张谨



