2015年10月27日,Cell杂志子刊Cell Reports以封面特色形式发表了模式动物研究所杨中州实验室和北京大学医学部王文恭实验室的合作论文“Post-transcriptional regulation of Nkx2-5 by RHAU in heart development”,该研究揭示了心脏发育关键基因Nkx2-5的转录后调控新机制。
G-四链体(G-quadruplexes, G4s)是由富含鸟嘌呤(GGG)形成的二级结构,存在于DNA或RNA序列当中。近年来的研究发现,RNA分子中 G-四链体主要定位在mRNA的5′和3′非翻译区(UTRs)。RNA G-四链体在RNA生物学,比如RNA剪切加工,成熟,运输及翻译中发挥重要调控作用。人类转录组中大约有3000个基因的mRNA 5′ UTR中包含G-四链体序列,提示G-四链体有可能是mRNA生物学调控的通用调控结构。
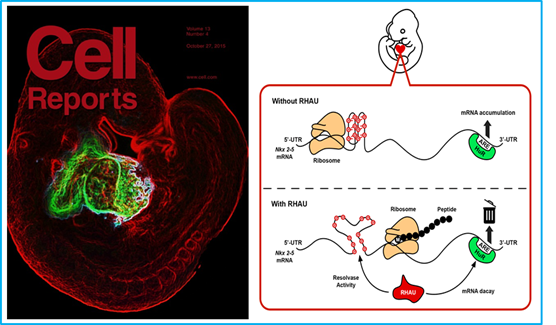
以前的研究发现,RNA结合蛋白RHAU可以结合G-四链体,将其打开,但参与的生物学功能尚不明了。在小鼠中剔除Rhau会导致胚胎死于第7.5天左右,证明RHAU对早期胚胎发育至关重要,并提示在器官发育过程中可能发挥关键作用。为了研究RHAU在心脏发育过程中的功能,杨中州实验室在心脏祖细胞中将Rhau剔除,发现剔除小鼠发生胚胎致死,心脏发育出现异常,证明RHAU对胚胎心脏发育不可或缺。通过生化及分子生物学实验分析,发现RHAU可以结合心脏发育关键基因Nkx2-5 mRNA的5’及3’ UTR(非翻译区域),调控mRNA稳定性(代谢)及蛋白质翻译。RHAU结合Nkx2-5 mRNA的3’ UTR中的ARE元件促进Nkx2-5 mRNA降解,而结合Nkx2-5 mRNA的5’ UTR中的G4二级结构,将其打开,促进蛋白质翻译。Rhau剔除小鼠心脏组织中,Nkx2-5 mRNA水平虽然升高,但Nkx2-5蛋白水平却显著降低。该研究阐述了Nkx2-5转录后调控的新机制,揭示了mRNA分子中非翻译区域中的调控元件及其功能。这项研究证实了mRNA 5′ UTR G-四链体介导的蛋白质翻译在器官发生中的作用。
杨中州教授和王文恭教授是这篇论文的共同通讯作者,博士生聂俊伟与江明扬为共同第一作者。
该研究得到科技部和自然基金委的项目支持。