2026年3月26日,来自中国科学院上海营养与健康研究所的张俊兵研究员应邀访问南京大学模式动物研究所,为全所师生做了题为“Deciphering the cysteinome in cancer”的学术报告。
张俊兵博士毕业于北京生命科学研究所;此后在美国哈佛大学医学院附属麻省总医院进行博士后研究;于2024年受聘为美国哈佛大学医学院讲师;2025年全职回国加入中国科学院上海营养与健康研究所。他研究组主要聚焦“肿瘤代谢与翻译后修饰”,通过结合一系列前沿高通量技术,如CRISPR遗传筛选、碱基编辑筛选、代谢组学和定量化学蛋白质组学等,深入探索细胞代谢异常与癌症、衰老相关疾病之间的关系。长期研究目标是鉴定癌症及衰老相关疾病中的可成药靶点与代谢相关的致命弱点。
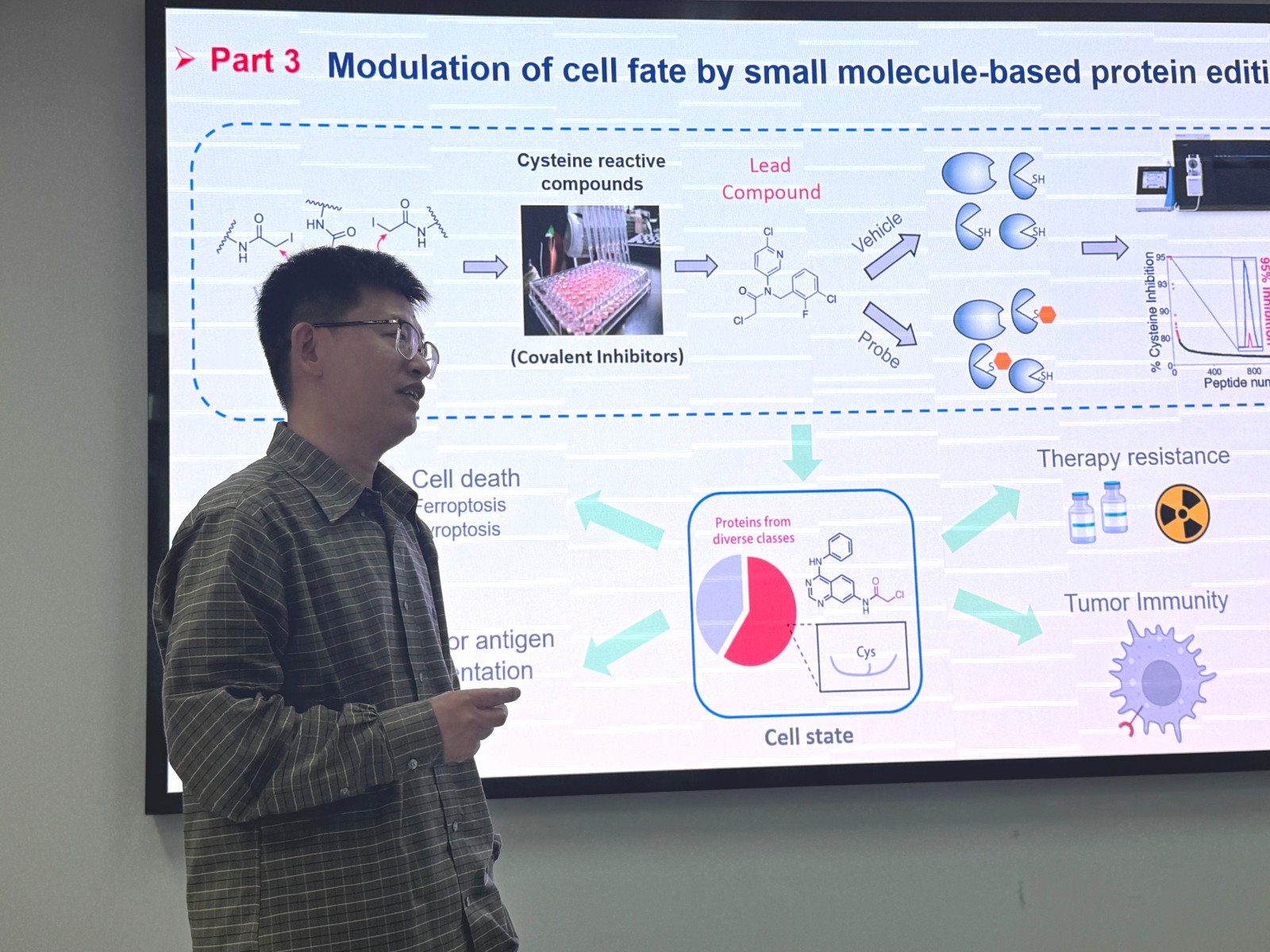
化疗药物常通过升高肿瘤细胞内活性氧水平来杀死癌细胞,但癌细胞也演化出了一套精密的“抗氧化”感知系统。张俊兵团队发现,这一系统的核心是半胱氨酸——其巯基对氧化极其敏感,如同一个“分子开关”。为系统寻找具体的关键开关,团队整合了多种高通量筛选技术:2023年的 《Cell》 工作中,他们利用基于半胱氨酸的化学蛋白质组学和全基因组CRISPR遗传筛选,绘制了超过35,000个半胱氨酸的反应图谱,鉴定出DNA损伤激酶CHK1是核心调控因子;2025年的 《Nature》 研究中,他们进一步采用碱基编辑筛选系统结合细胞膜蛋白质组学,发现逆转录复合体蛋白VPS35上的两个关键半胱氨酸(C653/C673),其一旦突变,细胞就会对多种化疗药物产生耐药。
两条通路殊途同归:在细胞核内,CHK1的第408位半胱氨酸被氧化后激活,进而抑制SSBP1介导的线粒体翻译;在细胞膜上,VPS35被氧化后导致精氨酸转运蛋白SLC7A1从膜上解离,抑制精氨酸的摄取,降低线粒体翻译。线粒体翻译正是细胞调控氧化应激的总开关。
这一机制在肿瘤化疗耐药中扮演关键角色。张俊兵团队发现,VPS35或SSBP1表达水平越低的卵巢癌患者,对铂类化疗的耐药性越强,肿瘤复发越快。这提示肿瘤细胞正是通过“劫持”这一通路来抵御化疗。这些工作为癌症的精准治疗提供了新思路:CHK1和VPS35或可作为预测化疗疗效的潜在标志物,这些功能关键的半胱氨酸,也为开发新型靶向药物提供了精确位点。

张俊兵研究员的讲座引发师生热烈讨论,大家踊跃提问,他细致解答,给在场师生带来诸多启发。
文字编辑:贾玉环
图片拍摄:贾玉环
责任编辑:张谨



